Σήμερα, η Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) έδωσε πρώιμη έγκριση στο Oxbryta (voxelotor) για τη θεραπεία της δρεπανοκυτταρικής νόσου (SCD) σε ενήλικες και παιδιά 12 ετών και άνω.
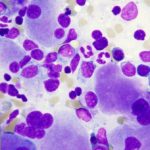
Η δρεπανοκυτταρική νόσος ή δρεπανοκυτταρική αναιμία, είναι ένα γενετικό νόσημα, στο οποίο τα ερυθρά αιμοσφαίρια αποκτούν ανώμαλο σχήμα (κάτι σαν ημισέληνο ή “δρεπανοειδές”), και αυτή η κατάσταση δυσχεραίνει τη ροή του αίματος στα αγγεία και περιορίζει την παροχή οξυγόνου στους ιστούς, οδηγώντας σε βλάβη οργάνων. Χαρακτηρίζεται επίσης από σοβαρή και χρόνια φλεγμονή, που επιδεινώνει τις επώδυνες κρίσεις, κατά τη διάρκεια των οποίων οι ασθενείς εμφανίζουν επεισόδια έντονων πόνων και βλάβης οργάνων. Οι πρώτες μη κλινικές μελέτες έδειξαν ότι το Oxbryta βελτιώνει την ροή του αίματος κάνοντας τα ερυθρά αιμοσφαίρια πιο ελαστικά και λιγότερο ευπαθή στη μηχανική παραμόρφωση.
Η έγκριση του Oxbryta βασίστηκε στα αποτελέσματα μιας κλινικής μελέτης σε 274 ασθενείς με δρεπανοκυτταρική νόσο, στην οποία 51,1% ασθενών που έλαβαν 1500 mg Oxbryta για 6 μήνες βελτίωσαν την αιμοσφαιρίνη τους κατά 1gr/dL, σε σχέση με 6,5% ασθενών που έλαβαν εικονικό φάρμακο.
Το Oxbryta έλαβε ταχεία έγκριση, διαδικασία που επιτρέπει στο FDA να εγκρίνει φάρμακα για σοβαρές καταστάσεις στις οποίες υπάρχει κενό θεραπείας και ανάγκη για αποτελεσματικά φάρμακα, με βάση ένα αποτέλεσμα που δεν είναι μεν τεκμηριωμένο, αλλά είναι αρκετά πιθανό να προσφέρει κλινικό όφελος στους ασθενείς.